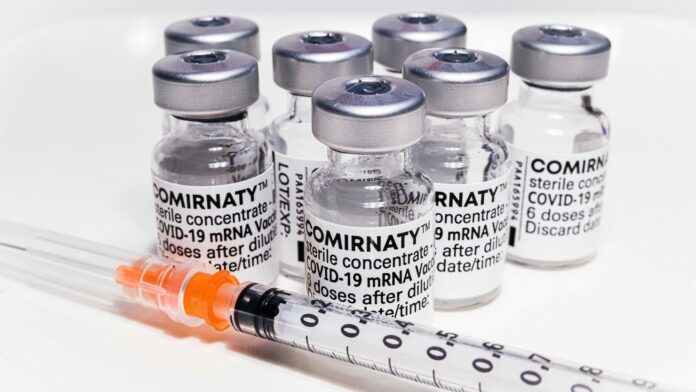
Wie die beiden Unternehmen Pfizer Inc. und BioNTech am gestrigen Montag (04.10.2021) bekannt gaben, hat der Ausschuss für Humanarzneimittel (Committee for Medicinal Products for Human Use, CHMP) der Europäischen Arzneimittel-Agentur (European Medicines Agency, EMA) eine positive Beurteilung zur Verabreichung des COVID-19 Impfstoffs der Unternehmen als Auffrischungsdosis mindestens sechs Monate nach der zweiten Dosis für alle Personen ab 18 Jahren abgegeben hat.
Entscheidung der Europäischen Kommission steht noch aus
Die Europäische Kommission (EK) wird die CHMP-Empfehlung prüfen und voraussichtlich in Kürze eine Entscheidung über eine Änderung der bedingten Marktzulassung treffen. Wenn die EK die Änderung der bedingten Zulassung in Bezug auf eine Auffrischungsimpfung (dritte Dosis) genehmigt, gilt die Entscheidung sofort für alle 27 EU-Mitgliedstaaten.
Verschiedene Daten als Grundlage
Die positive Beurteilung durch das CHMP basiert auf Ergebnissen der klinischen Studien von Pfizer-BioNTech, Daten aus der praktischen Anwendung sowie Literaturdaten. Die von Pfizer und BioNTech eingereichten klinischen Studiendaten umfassen die Evaluierung der Sicherheit, Verträglichkeit und Immunogenität einer Auffrischungsimpfung mit COMIRNATY®. Verglichen mit den Werten nach der zweifachen Impfung zeigte eine Auffrischungsimpfung signifikant höhere neutralisierende Antikörpertiter gegen das ursprüngliche SARS-CoV-2 Virus (Wildtyp) sowie gegen die Beta- und Delta-Varianten. Das Reaktogenitätsprofil war innerhalb der ersten sieben Tage nach der Auffrischungsimpfung im Allgemeinen mild bis moderat und die Häufigkeit der Impfreaktionen war vergleichbar oder geringfügiger als nach der zweiten Dosis. Das Nebenwirkungsprofil entsprach im Allgemeinen den bisherigen klinischen Sicherheitsdaten von COMIRNATY.
Mutmaßlich keine Auswirkung auf bestehende Liefervereinbarungen
Pfizer und BioNTech werden im Rahmen der bestehenden Liefervereinbarung mit der EK den Impfstoff, einschließlich ausreichender Mengen für Auffrischungsimpfungen, weiter ausliefern. Die Unternehmen gehen davon aus, dass die Einführung der Auffrischungsimpfungen in den Vereinigten Staaten und der EU, falls genehmigt, keine Auswirkungen auf bestehende Liefervereinbarungen mit anderen Regierungen weltweit und internationalen Gesundheitsorganisationen haben wird.
COMIRNATY basiert auf BioNTechs unternehmenseigener mRNA-Technologie und wurde von BioNTech und Pfizer gemeinsam entwickelt. BioNTech ist Inhaber der Marktzulassung in den Vereinigten Staaten, der Europäischen Union, dem Vereinigten Königreich und Kanada sowie Inhaber von Notfallzulassungen und weiterer Zulassungen in den Vereinigten Staaten (gemeinsam mit Pfizer) und anderen Ländern. Ergänzende Anträge auf Arzneimittelzulassung in den Ländern, in denen ursprünglich Notfallgenehmigungen oder gleichwertige Genehmigungen erteilt wurden, sind in Bearbeitung.
GENEHMIGTE ANWENDUNG IN DER EU:
COMIRNATY® ▼ (der COVID-19-Impfstoff von Pfizer-BioNTech) hat von der Europäischen Kommission (EK) die bedingte Zulassung zur Prävention der Coronavirus-Erkrankung 2019 (COVID-19) bei Menschen ab 12 Jahren erhalten. Der Ausschuss für Humanarzneimittel (CHMP) der EMA hat seine sorgfältige Bewertung von COMIRNATY® abgeschlossen und ist im Konsens zu dem Schluss gekommen, dass nun ausreichend belastbare Daten zur Qualität, Sicherheit und Wirksamkeit des Impfstoffs vorliegen.
WICHTIGE SICHERHEITSINFORMATIONEN:
- Es wurden Fälle von Anaphylaxie berichtet. Für den Fall einer anaphylaktischen Reaktion nach der Verabreichung des Impfstoffs sollte immer eine angemessene medizinische Behandlung und Überwachung bereitstehen.
- Sehr selten wurde bei Personen, die den Impfstoff erhalten haben, eine Myokarditis (Entzündung des Herzmuskels) und Perikarditis (Entzündung des Herzbeutels) beobachtet. Bei den meisten dieser Personen begannen die Symptome innerhalb von 14 Tage nach der Impfung, häufiger nach Erhalt der zweiten Impfstoffdosis und häufiger bei jungen Männern.
- Im Zusammenhang mit der Impfung selbst können Angstreaktionen wie vasovagale Reaktionen (Synkopen), Hyperventilation oder Stressreaktionen (z. B. Schwindel, Herzklopfen, Anstieg der Herzfrequenz, Blutdruckveränderungen, Kribbeln und Schwitzen) auftreten. Stressbedingte Reaktionen sind vorübergehend und klingen von selbst wieder ab. Die Betroffenen sollten darauf hingewiesen werden, dass sie ihre Symptome dem Impfarzt melden sollten, damit dieser sie untersuchen kann. Es ist wichtig, dass Vorkehrungen getroffen werden, um Verletzungen durch Ohnmacht zu vermeiden.
- Die Wirksamkeit, Sicherheit und Immunogenität des Impfstoffs wurde bei immungeschwächten Personen, einschließlich Personen, die eine immunsuppressive Therapie erhalten, nicht untersucht. Die Wirksamkeit von COMIRNATY® kann bei immunsupprimierten Personen geringer sein.
- Wie bei jedem Impfstoff schützt die Impfung mit COMIRNATY® möglicherweise nicht alle Empfänger des Impfstoffs. Personen sind möglicherweise erst 7 Tage nach ihrer zweiten Impfdosis vollständig geschützt.
- Die häufigsten Nebenwirkungen bei den Studienteilnehmern im Alter von 16 Jahren oder älter waren Schmerzen an der Injektionsstelle (> 80 %), Müdigkeit (> 60 %), Kopfschmerzen (> 50 %), Muskelschmerzen und Schüttelfrost (> 30 %), Arthralgie (> 20 %), Pyrexie und Schwellungen an der Injektionsstelle (> 10 %), die in der Regel leicht oder mäßig ausgeprägt waren und innerhalb weniger Tage nach der Impfung abklangen. Die Häufigkeit der Nebenwirkungen war mit höherem Alter etwas geringer.
- Das allgemeine Verträglichkeitsprofil von COMIRNATY® bei Geimpften im Alter von 12 bis 15 Jahren war vergleichbar mit dem bei Geimpften im Alter von 16 Jahren oder älter. Die häufigsten Nebenwirkungen bei den 12- bis 15-jährigen Studienteilnehmern waren Schmerzen an der Injektionsstelle (> 90 %), Müdigkeit und Kopfschmerzen (> 70 %), Muskelschmerzen und Schüttelfrost (> 40 %), Gelenkschmerzen und Fieber (> 20 %).
- Es liegen nur begrenzte Erfahrungen mit der Anwendung von COMIRNATY® bei schwangeren Frauen vor. Die Verabreichung von COMIRNATY® in der Schwangerschaft sollte nur in Betracht gezogen werden, wenn der mögliche Nutzen die möglichen Risiken für Mutter und das ungeborene Kind überwiegt.
- Es ist nicht bekannt, ob COMIRNATY® in die Muttermilch übergeht.
- Wechselwirkungen mit anderen Arzneimitteln oder die gleichzeitige Verabreichung von COMIRNATY® mit anderen Impfstoffen sind nicht untersucht worden.
- Die vollständigen Sicherheitsinformationen zu COMIRNATY® sind in der zugelassenen Zusammenfassung der Merkmale des Arzneimittels und der Arzneimittelinformation zu finden. Diese sind in allen Sprachen der Europäischen Union auf der Webseite der EMA zu finden.
Zusätzliches Monitoring erforderlich
Das schwarze gleichseitige Dreieck ▼ bedeutet, dass ein zusätzliches Monitoring erforderlich ist, um eventuelle unerwünschte Reaktionen zu erfassen. Dies ermöglicht eine schnelle Identifizierung von neuen Sicherheitsinformationen. Einzelpersonen können helfen, indem sie alle Nebenwirkungen, die sie bekommen, melden. Nebenwirkungen können an EudraVigilance oder direkt an BioNTech per E-Mail medinfo@biontech.de, Telefon +49 6131 9084 0 oder über die Website www.biontech.de gemeldet werden.
Notfallzulassung zur Prävention
Notfallverwendungen des Produktes wurden nicht durch die FDA zugelassen oder lizensiert, sondern im Rahmen einer Notfallzulassung (Emergency Use Authorization, „EUA“) zur Prävention der Coronaviruserkrankung 2019 (COVID-19) bei Personen ab 12 Jahren genehmigt. Die Notfallzulassungen im Rahmen der EUA sind nur für die Dauer der Erklärung zulässig, in der Umstände vorliegen, die die Genehmigung einer Notfallzulassung des Medizinproduktes gemäß Abschnitt 564(b)(1) des FD&C Act rechtfertigen, es sei denn, die Erklärung wird früher beendet oder die Genehmigung widerrufen. Das EUA Informationsblatt kann abgerufen werden unter www.cvdvaccine-us.com.